龙德医疗器械服务集团
龙德医疗器械服务集团
- 集团介绍
- 集团新闻
- 集团成员
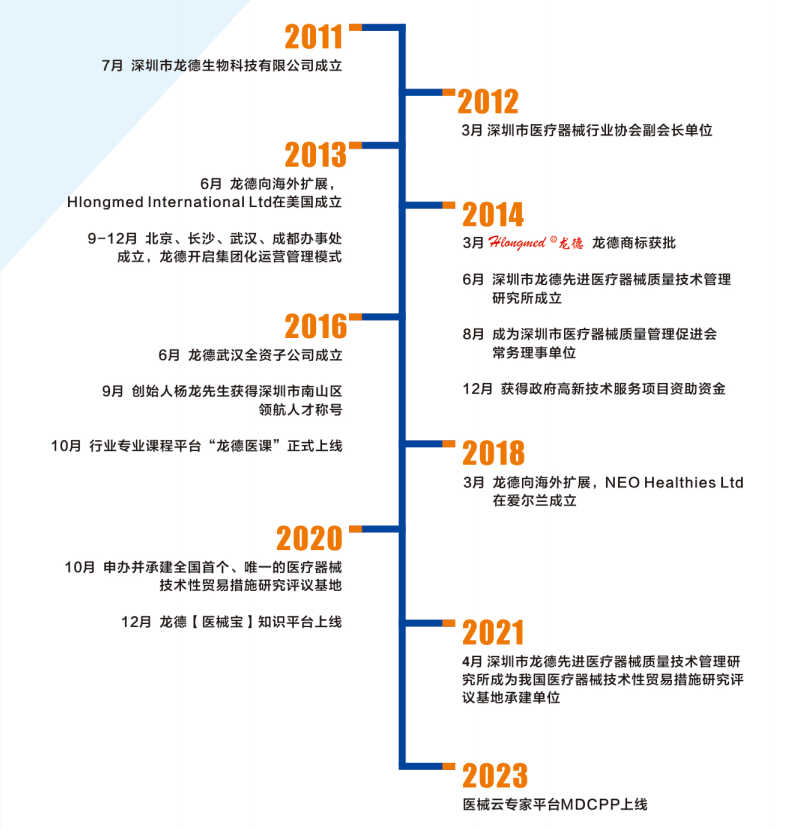
- 发展历程
- 主营业务
- 主要客户
- 联系我们
龙德是专业领先的医疗器械法规合作伙伴、CDMO、临床试验CRO/CRA/SMO/CRC合作组织和值得信赖的专业医疗器械行业整体解决方案及CDMO服务商。
龙德总部位于深圳,在美国、爱尔兰、香港、越南、加纳、新加坡、北京、武汉、苏州、长沙、成都和重庆等地拥有子公司或办事机构,并在深圳设有一个专业研究所。服务范围辐射全球,合作伙伴来自北美、欧洲、中国等多个国家和地区,现已为超过3000多家企业、政府机构、医院、第三方监管机构、认证机构及非盈利组织提供专业服务。
龙德核心团队成员均来自长期从事医疗器械临床试验、CDMO、法规注册、质量体系管理等领域工作的资深人士及专家,拥有丰富的医疗器械临床试验、法规注册、质量体系及流程优化等理论知识,及多年的实践经验。龙德与全球众多临床试验机构、公告机构、主管当局、测试机构、协会、投资机构、知识产权及法律机构长期保持着友好关系。

龙德生物:深圳市龙德生物科技有限公司
龙德咨询:深圳龙德医疗器械咨询有限公司
深圳:深圳龙威咨询有限公司
深圳:深圳市鸿鑫卓越管理技术有限公司
南京:南京龙德汇海科技服务有限公司
香港:香港科大龍德生物科技有限公司
龙德研究所:深圳市龙德先进医疗器械质量技术管理研究所
美国: Hlongmed International Ltd.
越南:GENIUS CARGO JSC
加纳:HCOWA GHANA LIMITED COMPANY
新加坡:HLONGMED SINGAPORE PTE. LTD.
澳大利亚:HLONGMED AUSTRALIA PTY LTD.
欧洲爱尔兰:NEO HEALTHIES LTD.






联系电话:0755-86664989
联系邮箱:consultant@hlongmed.com
地址:广东省深圳市南山区高新区北区乌石头路8号天明科技大厦16楼
龙德生物:深圳市龙德生物科技有限公司 美国:Hlongmed International Ltd.
龙德咨询:深圳龙德医疗器械咨询有限公司 越南:GENIUS CARGOJSC
深圳:深圳市鸿鑫卓越管理技术有限公司 加纳:HCOWA GHANA LIMITED COMPANY
深圳:深圳龙威咨询有限公司 新加坡:HLONGMED SINGAPORE PTE. LTD.
香港:香港科大龍德生物科技有限公司 欧洲爱尔兰:NEO HEALTHIES LTD.
龙德研究所:深圳市龙德先进医疗器械质量技术管理研究所

