【线下第十一期】8月21日体外诊断试剂临床试验设计经验分享会
【国际医疗器械合规联盟线下分享会】- 第十一期
8月21日|体外诊断试剂临床试验设计经验分享会
【活动背景】
随着体外诊断试剂在临床检测和疾病管理中的应用日益广泛,其临床试验设计的重要性也愈发凸显。对于研发人员和相关企业而言,设计一个科学、规范的临床试验是确保产品能够有效进入市场并获得临床认可的必要前提。
体外诊断试剂的临床试验设计通常涉及以下几个核心问题:
1.哪些产品属于体外诊断试剂?
2.体外诊断试剂有哪些监管要求?
3.体外诊断试剂是否需要开展临床试验?
4.体外诊断试剂临床试验有哪些需要注意的关键点?
5.体外诊断试剂临床试验有哪些常见问题?
为了更好地应对这些问题,我们临床专家团队,基于体外诊断试剂的相关法规要求,结合多年的临床试验经验,将围绕体外诊断试剂的临床试验设计、实施及数据分析,进行深入的解读和分享,助力相关企业在体外诊断认证过程中取得成功。期待并欢迎大家的积极参与及交流!
龙德推出【国际医疗器械合规联盟线下分享会】系列活动,以服务和帮助中国医疗器械产业,共绘全球医疗健康新篇章!期待您的参与!
【参会对象】
企业、医疗机构、高等院校、科研单位等从事医疗器械研发、注册、企业运营、市场销售等相关工作的人员;感兴趣学习的从业人员。
【主办机构】
龙德医疗器械服务集团
国际医疗器械法规合规联盟
【协办机构】
龙德先进医疗器械质量技术管理研究所
深圳市龙德生物科技有限公司
【参会具体事项】
1.时间:2024年8月21日 14:00-15:45(初拟时间)
2.规模:30人,报满即止。
3.地点:深圳市南山区西丽街道松坪山社区乌石头路8号天明科技大厦16楼会议室
【收费标准】
1.医械云专家平台、医械宝、龙德医课直播间会员,参会免费;
2.国际医疗器械合规联盟发起单位、会员单位、联盟个人发起人和联盟会员:1个免费名额(企业或个人申请加入国际医疗器械合规联盟可联系龙德医课微信:hlongmed88)
3.其余参会人员200元。
【参会议程】
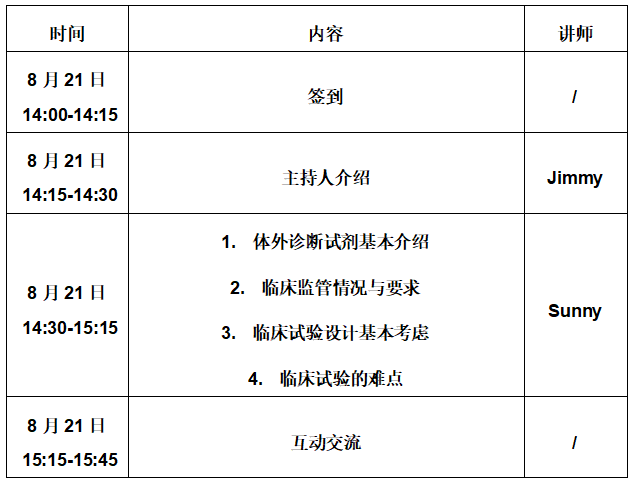
【线下系列活动计划表】

【参会方式】
1.点击下方链接或扫描下方二维码,填写报名表。本次培训报名截止时间为2024年8月9日12:00。名额有限,报满即止。
报名链接:https://docs.qq.com/form/page/DY0VMam5uQ1ZUSk95
报名二维码:

特别说明:①请确保填写信息完整、真实,否则可能无法审核通过;
②8月21日前将以手机短信、微信形式发送确认信息,请密切关注并及时回复确认。
2.活动联系人:
赵女士:13560790058
陈先生:19166267960
【付款方式:网银转账】
其他参会人员,请于8月21日12:00前将费用转账至如下指定银行账户。(缴费时请备注公司或人员姓名)
账户名称: | 深圳市龙德生物科技有限公司 |
账 号: | 7653 5794 2019 |
开户行: | 中国银行股份有限公司深圳东滨路支行 |
【开票信息】
1.缴费后,一周内开具【普通电子发票】,并发送至报名邮箱。
2.请提供发票信息:
1)发票抬头;
2)单位税号;
3)选择发票内容(会务费/咨询费)。
3.发票信息请发送至活动联系人邮箱cjm@hlongmed.com。


