重磅来袭!欧盟MDR临床评价实战工作坊课程(附优惠通道)
——理论奠基|实战拆解|案例众创|长期陪跑
龙德医疗器械服务集团专家团队打造|优惠通道限时开放
为什么本课程是您突破临床评价壁垒的最佳选择?
欧盟临床评价是MDR认证最难的部分之一,国内制造企业普遍面临三大核心瓶颈:
➤ 法规框架混淆:文档结构被公告机构判定为“系统性缺陷”导致发补,企业对于如何优化文档结构,如何补充正文内容不知所措!
➤ 技术方法论缺失:SOTA阈值缺乏统计学支撑、缺少临床参数、等同比对参数映射逻辑断裂,相关发补问题处理困难!
➤ 资源渠道封闭:头部企业资料模板加密管控、欧盟专家咨询成本超高、EUDAMED数据库访问受限,对比产品说明书等资料文档访问困难!
系统学习本课程,您将实现三大能力跃迁:
✅ 知识体系重构:20+小时线上精讲拆解,全方位掌握临床评价底层基础逻辑
✅ 实战能力突破:线下工作坊直击临床评价真实案例,专家现场解答临床评价真实案例、与企业一线业务同事共同应对临床评价关键问题
✅ 资源网络贯通:加入临床评价专业社群,全程在线专业辅导
课程体系全景图
第一阶段:线上系统精讲(20+小时必修课)
模块1:临床评价主要法规要求
MDR法规对临床评价的要求
MDCG等指南对临床评价的要求
模块2:临床评价方案(CEP)设计
概述、定义及识别通用安全与性能要求
识别器械预期用途及适应症
确定患者收益描述及临床结果参数
SOTA文献检索
临床益处和临床性能的考虑及验收标准
临床安全性的定性和定量的方法以及剩余风险和副作用的确定
建立风险收益可接受的指标清单、说明及临床开发计划
模块3:临床评价报告(CER)撰写
相关法规/指南介绍-临床评价有哪些阶段/流程如何?
编写要求及示例
模块4:上市后监督与跟踪
上市后监督(PMS)
定期安全更新报告 (PSUR)
CE MDR上市后临床跟踪(PMCF)
第二阶段:线下案例攻坚专题工作坊
特色1:真实案例众创
学员可携带临床评价真实案例探讨处理方案(脱敏处理后现场演示)
学员预先提交三个及以上临床评价重点关切问题,进行针对性研讨
特色2:行业内重点关切问题深度覆盖
问题板块:根据现场工作坊讨论,可能涉及到临床评价最核心的这些难点:
1.SOTA的定义与应用
2.SOTA构建标准化步骤
3.医疗状况与疾病自然过程描述
4.等同比对法规要求与策略
5.等同产品选择与对比表设计
6.医疗器械软件等同对比路径
7.等同产品参数缺失的解决方案
8.临床评价路径识别与选择
9.临床参数向临床获益转化
10.PICO检索词优化策略
11.SOTA文献检索
12.CER文献检索
13.文献质量如何评价
14.文献参数不足的数据补充策略
15.CER用户手册警告条款合规呈现
16.非欧盟标准数据的合规处理
17.临床试验是否符合ISO 14155:2020
18.宣传手册宣称内容合规管理
19.PMCF Plan被拒可能的问题和修正方法
20.PMCF计划设计与认可要点
21.医疗器械机构登记册数据检索
22.等同器械CE证书缺失的替代证明
23.持续增加.....
课程专属权益
培训收获
★《欧盟MDR临床评价实战培训》培训证书(至少参与一次线下实战工作坊后颁发)
★线上课程不限次回看学习
★全国巡回线下案例交流(小班制深度研讨)
★临床评价私享交流群(专家+同行实时互动)
课程优势
权威导师及专业团队领衔
领衔:龙德医疗器械服务集团创始人 杨龙先生
★香港科技大学客座教授、四川大学研究生产业导师
★具有丰富的CE注册、CE临床评价等综合经验
★拥有20多年的医疗器械国际法规研究、注册、临床评价和试验经验,运作超过上百个美国、欧盟、中国、澳大利亚、加拿大、巴西及日本等医疗器械法规研究、注册项目
★拥有20多年的医疗器械国际质量体系法规及标准研究、管理经验,辅导超百家医疗器械企业处理欧盟临床评价、顺利通过欧盟认证
专业团队:龙德注册一部和二部资深MDR临床评价项目经理及高级工程师团队亲自参与授课或者工作坊
龙德医疗器械服务集团丰富的项目经验背书
★集团累计完成数百个欧盟MDR临床评价项目,涵盖影像、诊断、治疗、植入器械、AI软件等各类产品类别
★辅导客户临床评价通过率高、效率高,文档质量优异
日程与报名
线上课程开放:2025.4.1
线下工作坊:第一次线下工作坊2025.4.11下午(天明科技大厦16楼会议室 · 小班制)
特别要求:
➤ 报名需提交 至少3个临床评价相关学习疑问
➤ 还需提供 1个用于讨论的临床评价实战案例
➤ 报名经审核通过后才具有报名资格
报名费用
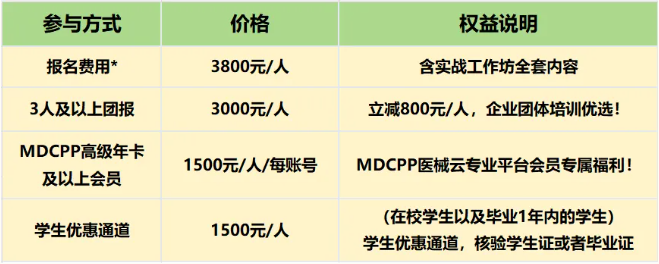
*报名费用包含:含线上课程听课权限、线下工作坊参与权限、临床评价私享交流群入群权限(需遵守群相关规则)。
扫码提交报名信息(附问题及实战案例),经我们审核后将给您发送确认报名成功的信息!

联系我们
微信:龙德医课 hlongmed88
联系电话:赵女士 13560790058
联系邮箱:consultant@hlongmed.com





